天津工生所解析链嗜酸菌来源二萜合酶催化机制
字号:【大】 【中】 【小】
微生物来源的二萜天然产物长期以来被认为是尚未充分开发的重要资源,在结构多样性与生物合成潜力方面仍具有广阔的挖掘空间。尤其是在放线菌中,二萜类化合物的生物合成能力尚缺乏系统性解析。链嗜酸菌属(Streptacidiphilus)作为一类嗜酸放线菌,其基因组中富含萜类合酶相关基因,但相关功能验证及产物类型研究仍相对有限。深入解析该类微生物来源二萜合酶的催化机制,将有助于拓展新型萜类骨架来源,并丰富生物催化酶资源体系。
近日,中国科学院天津工业生物技术研究所邓子新大师工作室系统解析了来源于链嗜酸菌Streptacidiphilus jiangxiensis的二萜合酶SjJS催化GGPP生成新型二萜类化合物jiangxidienes的环化机制及其后修饰路径。研究团队通过基因组挖掘鉴定获得萜类合酶SjJS,并结合体外酶催化实验与异源表达体系验证其功能。结果表明,该酶能够同时利用FPP和GGPP,分别生成倍半萜产物hedycaryol及新型二萜jiangxidiene A/B。为解析二萜形成过程中的复杂环化机制,研究采用位置特异性13C同位素标记策略,通过组合5种不同位置标记的异戊烯基焦磷酸(IPP)、异戊烯基焦磷酸异构酶(IDI)及多种异戊烯基转移酶,精确构建了GGPP全20个碳位点的标记体系,实现了对碳原子迁移路径的系统追踪。基于标记结果,研究明确捕捉到关键的C-19 甲基迁移事件,并提出两条可能的碳正离子级联环化路径。计算结果表明,两条路径在能量上均具可行性,但部分中间体的稳定性可能受到水分子参与的影响。进一步结合蛋白结构预测与分子动力学模拟,研究锁定了活性口袋中的关键残基,并通过定点突变验证其功能。结果显示,单点突变即可显著改变产物分布并拓展结构多样性,同时突变产物的结构特征为关键环化路径提供了实验支持。此外,邻近的细胞色素P450被证实参与主产物的选择性氧化修饰,并对分离获得的化合物进行了抗肿瘤活性评价。
该研究获得国家重点研发计划、国家自然科学基金、合成生物学海河实验室创新及重点项目以及天津市合成生物技术创新能力提升行动等项目的支持。相关成果已发表于Chinese Chemical Letters。客座硕士研究生阎勃陶为论文第一作者,中国科学院天津工业生物技术研究所侯安伟研究员、徐敏研究员以及广西民族大学姜明国教授为共同通讯作者。
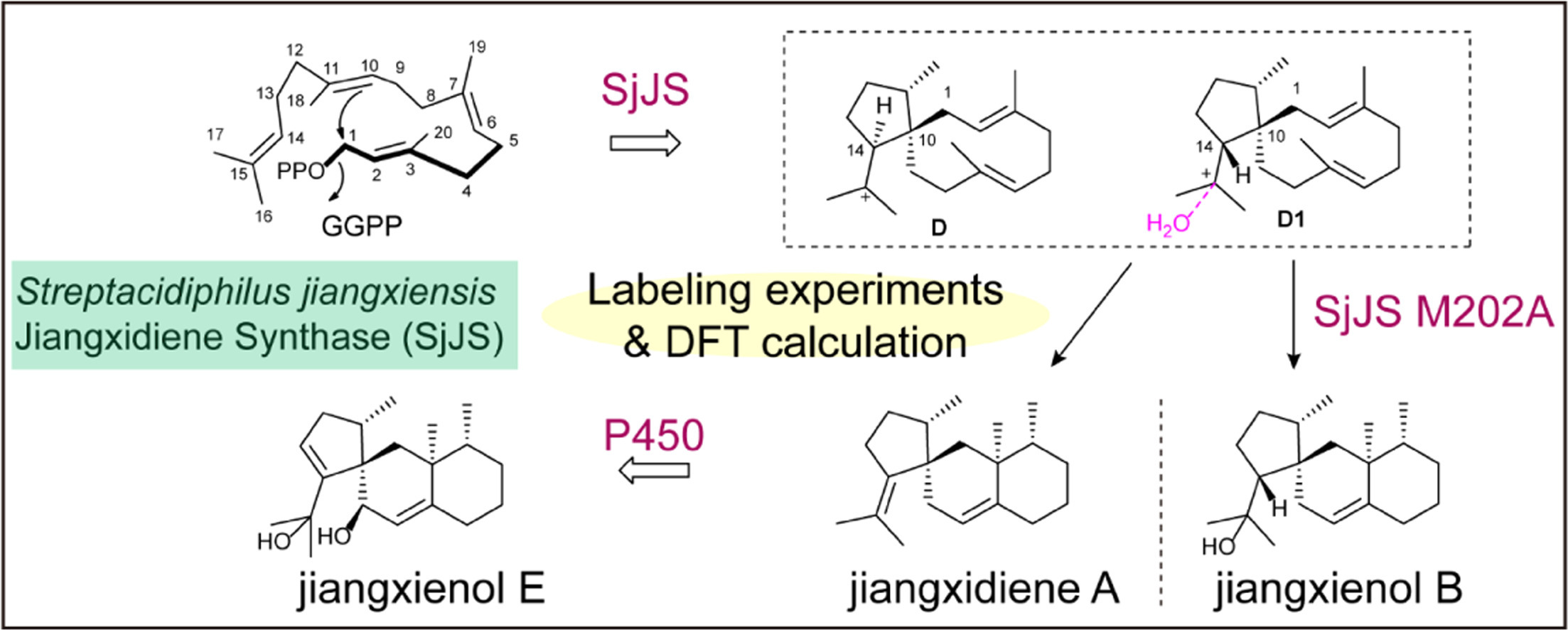
同位素标记、DFT计算和突变分析共同揭示了由二萜合酶SjJS催化的碳正离子环化级联反应,同时其邻近的细胞色素P450对该酶产生的主要二萜产物进行氧化修饰
版权所有 © 2012- Copyright All Rights Reserved 中国科学院天津工业生物技术研究所 版权所有
通讯地址:天津空港经济区西七道32号,邮编:300308
电话:022-84861997/84861977,传真:022-84861926,邮箱:tib_zh(AT)tib.cas.cn