天津工生所在酶立体选择性反转的计算模拟设计研究方面取得新进展
字号:【大】 【中】 【小】
酶的对映选择性控制是合成生物学与酶工程领域长期面临的技术瓶颈,尤其是在复杂底物或非天然构型的高选择性获取方面更具挑战。尽管CAST、ISM、FRISM等传统理性设计策略在改造酶立体选择性上取得一定进展,但由于候选空间巨大、协同效应复杂,迭代步骤中往往涉及湿实验验证。近年来,分子对接、动力学模拟及Rosetta等计算工具不断发展,使得酶的选择性预测精度有所提升,但“在不依赖中间步骤湿实验验证的前提下,完全通过计算预测设计多重突变位点的立体选择性”仍是行业难题。
近日,中国科学院天津工业生物技术研究所孙周通研究员带领团队在醇脱氢酶立体选择性反转的全计算模拟设计方面取得关键突破。该研究围绕源自嗜热微生物的TbSADH构建了一套多模块集成的酶选择性虚拟设计平台,成功预测并获得对映选择性完全翻转的三突变体(M3-1),将酶对底物4-苯基-2-丁酮的立体选择性从S(99% ee)反转为R(99% ee)。该工作为多突变酶理性设计提供了高效可行的计算范式,显著减少了实验筛选负担。
研究提出了三步式虚拟突变流程:首先,通过构象重塑与动力学模拟对底物结合口袋进行结构重构;其次,计算结合自由能并筛选亲和力更优突变体;最后引入NAC(近攻击构象)分析以验证催化构象在反应过程中的形成可能性。在该计算方法的支持下,团队聚焦三个关键Loop区域,发现第85位残基A85的缺失可显著拓展口袋体积并调控局部动态行为,构成选择性反转的核心驱动。进一步引入I86L和F112A突变,构建出三突变体M3-1,动力学分析显示其口袋体积提升41%,结合亲和力提高2.5倍,催化效率(kcat/Km)提升达140倍。M3-1在底物浓度50 mM和100 mM的200 mL体系中依然能保持高转化率和99% (R)立体选择性,且底物谱拓展实验显示其具备良好的广谱催化潜力。本研究首次建立了一个全计算驱动的多突变酶立体选择性设计体系,实现了从预测到验证的高效闭环流程,避免了突变体多轮设计中所涉及繁琐的湿实验验证步骤,为工业酶的功能重构提供了便捷途径。
该研究工作获得国家自然科学基金、天津市自然科学基金、国家重点研发计划及河北省重点研发计划支持。相关研究成果近日发表在国际学术期刊ACS Catalysis上。中国科学技术大学联合培养硕士研究生张博文与天津工生所博士后李聪聪为共同第一作者,孙周通研究员、Manfred T. Reetz教授与曲戈博士(现任华中农业大学教授)为共同通讯作者。
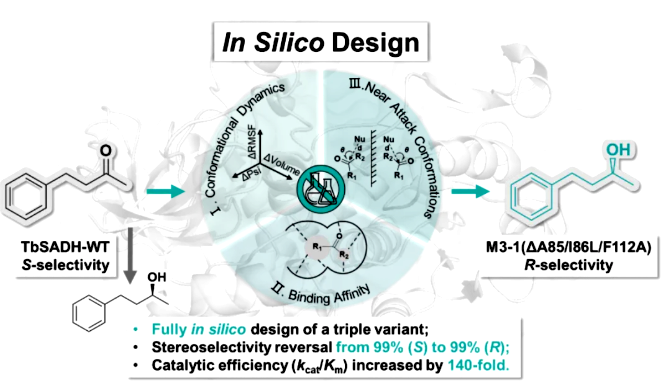
酶立体选择性反转的计算模拟设计流程示意图
版权所有 © 2012- Copyright All Rights Reserved 中国科学院天津工业生物技术研究所 版权所有
通讯地址:天津空港经济区西七道32号,邮编:300308
电话:022-84861997/84861977,传真:022-84861926,邮箱:tib_zh(AT)tib.cas.cn