一碳甲醇作为碳源生产饲用蛋白原料具有成本低、质量稳定可控等优点,一碳来源的单细胞蛋白被认为是食品和饲用蛋白质替代品。但是甲醇有毒性,甲醇代谢路径复杂,碳损失往往超过原料整体利用率的20%以上,无法实现甲醇代谢流高效定向转化为菌体蛋白,是制约甲醇蛋白合成经济性的主要技术瓶颈。
近日,中国科学院天津工业生物技术研究所吴信研究员带领的营养资源合成生物学研究团队在低值一碳原料生物合成单细胞蛋白方面取得新突破。团队通过组学解析毕赤酵母的甲醇代谢途径及关键节点,发掘了在甲醇胁迫条件下酵母细胞壁合成响应元件PAS_chr4_0305,定为解锁细胞壁感应器的人工靶标。研究发现在敲除PAS_chr4_0305后,细胞内海藻糖大量积累,表明细胞壁感应器被激活。进一步对毕赤酵母在激活细胞壁感应器后触发的调控机制进行了研究,借助组学数据检测到基因组层面的信号扰动相继通过HOG和CWI途径传导,引发毕赤酵母细胞壁重塑机制。进而毕赤酵母底盘在“内驱力”作用下的代谢流重编程,增强工业菌株对甲醇耐受度和代谢效率,大幅增强甲醇-蛋白代谢流的定向转化,提高碳氮协同转化效率并减少碳损失。最终实现毕赤酵母菌体干重和粗蛋白含量分别达到120 g/L和67.2%,甲醇-蛋白转化效率达到0.46 g DCW/g,达到理论值的92%,成功创制了具有自主知识产权、甲醇微生物蛋白高效合成的工业菌株。该研究将为解析毕赤酵母碳氮源高效利用与甲醇-蛋白质定向合成的调控机制提供新策略,也为突破甲醇蛋白生物制造经济阈值奠定基础。
该研究得到国家重点研发计划、中国科学院先导科技专项的支持,相关研究成果近期发表于Biotechnology for biofuels and bioproducts期刊,并获得授权发明专利2项。天津工业生物所副研究员高乐和博士后孟娇为论文共同第一作者,吴信研究员为论文通讯作者。
文章链接
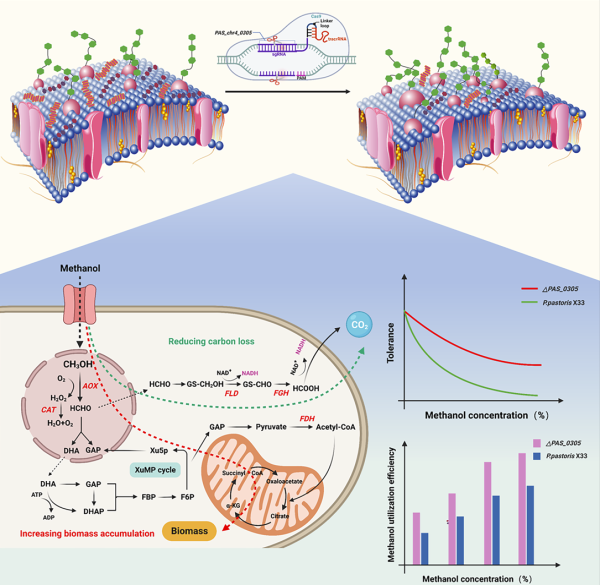
一碳甲醇定向生物合成微生物菌体蛋白的调控策略
