生物制造是以生物质等为原料,以菌种为工具工业化生产人类需要的食品、药品、化学品、材料、能源的绿色低碳生产方式,是推动新兴生物经济发展的重大战略方向。据预测,全球60%的产品可以用生物制造生产。在整个生物制造成本中,原料成本占了将近一半,因此提高产物的碳得率一直是生物制造的核心科技问题。
中国科学院天津工业生物技术研究所江会锋研究员带领的新酶设计与酵母基因组工程研究团队创建了能够高效利用C1-C6碳源的人工磷酸转酮酶路径(APK),为降低生物制造成本提供了新思路。乙酰辅酶A既是细胞生命中能量与物质代谢的枢纽,又是绝大多数生物制造产品的前体,在生命代谢网络中发挥着举足轻重的作用。自然糖降解路径从葡萄糖到乙酰辅酶A需要经过11步生化反应。科研人员以磷酸转酮酶(PK)为核心,设计了C1-C6碳源转化为乙酰辅酶A的人工磷酸转酮酶途径(APK),该途径仅仅需要3个核心酶就能够将C1-C6碳源完全转化为乙酰辅酶A。体外结果也证实人工磷酸转酮酶途径能够几乎无碳损的将C1-C6碳源转化为乙酰辅酶A,更进一步的实验也证明该途径在大肠杆菌体内可以发挥功能。
人工磷酸转酮酶(APK)途径突破了生物体自然进化局限,具有化学驱动力大、路线短、无需厌氧条件、没有碳损失等优点,不仅为探索早期地球生命起源提供借鉴,也有望在未来工业生物制造中发挥作用,具有重大的科学意义和实用价值。
该研究得到国家重点研发计划和国家自然科学基金等科技项目的资助。相关结果在线发表于国际学术期刊PLoS Biology。天津工业生物所博士研究生杨一群,副研究员刘玉万、博士研究生赵浩东和博士后刘丁玉为该文共同第一作者,江会锋研究员、马延和研究员为共同通讯作者。
文章链接
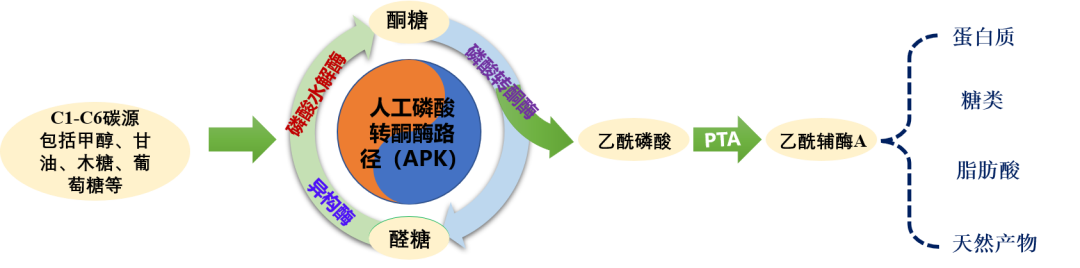
人工磷酸转酮酶途径
