合成生物学开辟了化学品人为设计合成的新境界,青蒿素生物合成颠覆植物提取路线是合成生物学的经典案例,组装操纵23个基因实现阿片类生物碱的生物合成,成为2015年世界十大科学突破之一。维生素B12是一种含有金属钴的复杂有机分子,广泛应用在药品、饲料、食品和化妆品等领域,需求逐年上升,市场缺口日益突出。微生物发酵是获得维生素B12的现有方式,发酵周期长、生产成本高,工业生产菌种遗传改造困难,提高产量难度极大。利用合成生物学手段,从头设计组装维生素B12合成途径、在异源细胞中实现生物合成,具有重大的科学与技术创新价值。但维生素B12结构复杂、合成途径长、关键基因缺失(图1),在异源细胞中操纵数十个基因、实现人工生物合成途径组装面临巨大挑战。
近日,中科院天津工业生物技术研究所张大伟研究员带领的蛋白表达系统与微生物代谢研究团队成功在大肠杆菌中实现了维生素B12的从头合成。研究人员首先解析了维生素B12好氧合成途径中钴螯合与腺苷钴啉醇酰胺磷酸的合成机理,然后将维生素B12合成途径划分成5个模块(图2),采用“自下而上”的策略将来源于Rhodobacter Capsulatus等5种细菌中的28个基因在大肠杆菌细胞中成功组装、调控,解决了多基因的适配机制问题,形成集成不同来源基因组装出的从头设计人工途径,最终实现了维生素B12的从头合成(图3),合成菌种发酵周期仅为目前工业生产菌株的1/10,有望成为新一代维生素B12工业菌株。这项研究不仅填补了维生素B12生物合成途径的缺口,而且成功实现了几十个基因在底盘细胞中有序的功能表达与调控,展示了模式菌株在异源复杂天然产物合成方面具有的巨大潜力,将启发和鼓励更多的复杂天然产物异源生物合成的研究。
该研究得到天津市和中国科学院相关项目支持,相关研究成果发表在国际权威期刊Nature Communications。中科院天津工业生物技术研究所助理研究员房欢博士为论文第一作者,张大伟研究员为论文通讯作者。
论文链接
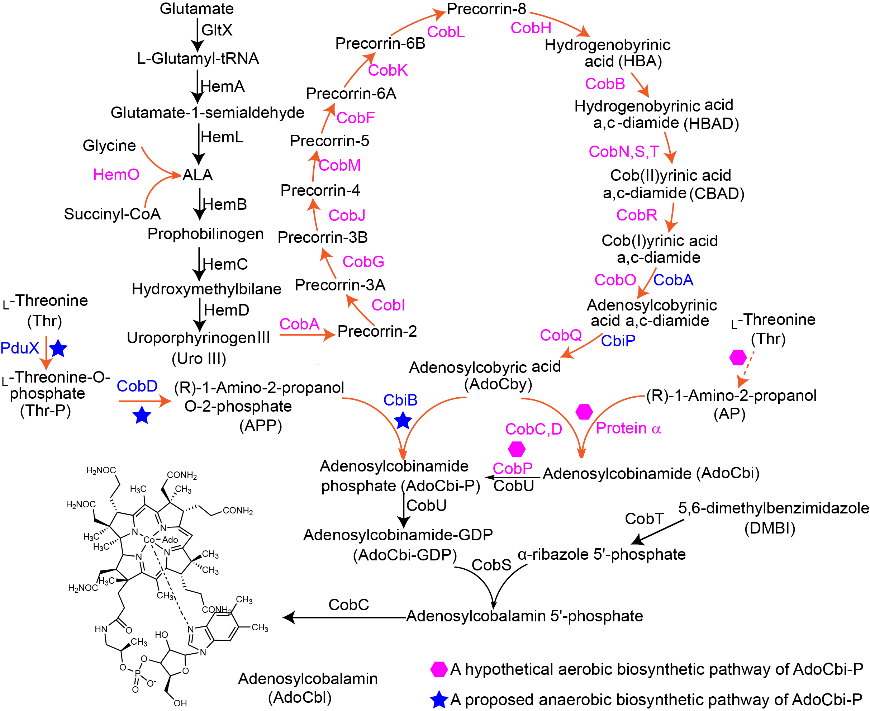
图1:维生素B12合成途径

图2:代谢工程改造大肠杆菌从头合成维生素B12
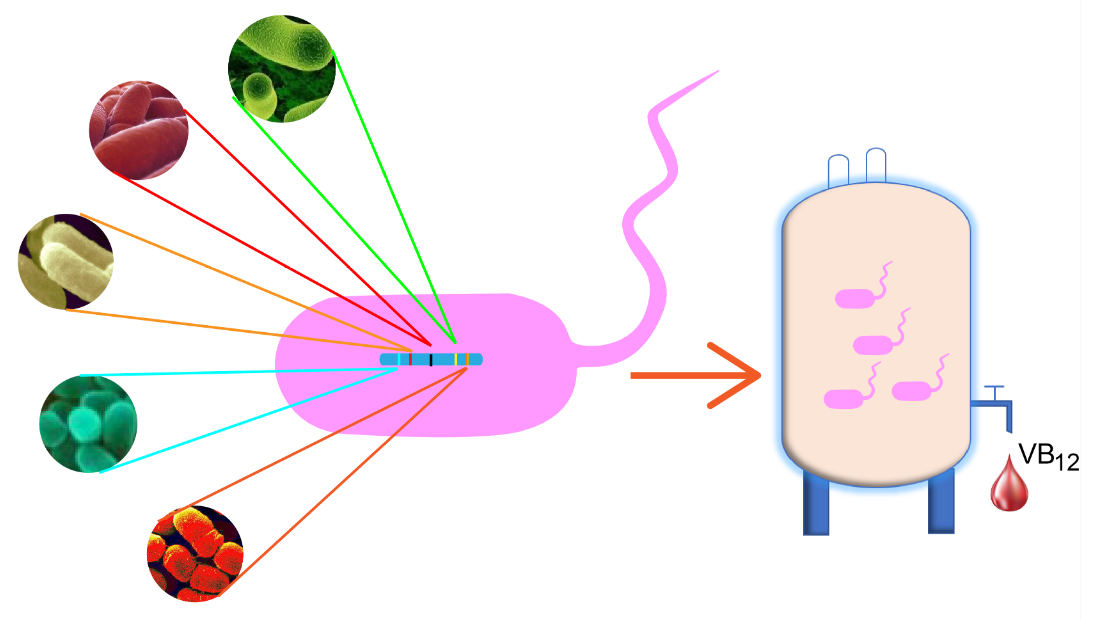
图3:5种不同来源共28个基因集成创建人工合成维生素B12途径
