L-稀少糖,具有重要生理功能,可用于防治肥胖、高血压、高血脂等疾病;此外,L-稀少糖还可以作为医药中间体合成L-核苷类药物,提高其抗肿瘤活性。然而,目前能够获得的L-稀少糖种类很少。
天津工业生物所功能糖与天然活性物质研究组通过代谢工程技术,构建了合成L-型稀少酮糖的工程菌,并成功合成了L-山梨糖和L-阿洛酮糖。科研人员首先挖掘了在C-C键的生物合成中具有广泛用途的果糖1,6-二磷酸醛缩酶(FruA)和塔格糖1,6-二磷酸醛缩酶(TagA),发现来源于大肠杆菌(Escherichia coli)的FruA和地衣芽孢杆菌(Bacillus licheniformis)的TagA催化磷酸二羟丙酮(DHAP)和L-甘油醛,出现产物构型非专一现象,获得两种产物L-山梨糖和L-阿洛酮糖。随后以谷氨酸棒杆菌为出发菌株,构建并优化了由FruA和去磷酸化酶(YqaB)组成的醛缩途径,以葡萄糖等为底物合成两种L-稀少己酮糖,通过代谢工程改造及发酵条件优化,提高了胞内DHAP和L-甘油醛的含量,产物得率进一步得到提高,最终L-山梨糖和L-阿洛酮糖产量为3.5g/L和2.3 g/L。该研究成果对于合成非天然构型的L-稀少糖提供了可借鉴的思路。
该研究获得国家“863”计划项目支持,相关研究成果已经发表在Applied and Environmental Microbiology期刊,天津工业生物所博士研究生杨建刚为第一作者。
文章链接
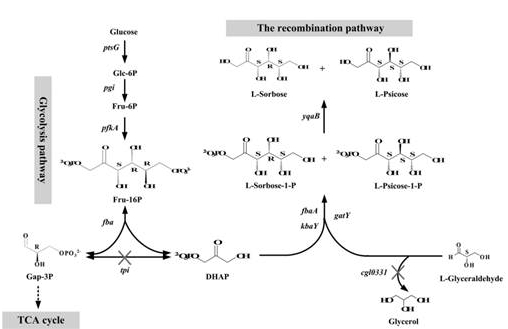
L-山梨糖/L-阿洛酮糖的微生物发酵生产策略
