天津工生所实现非天然孕激素从头合成
字号:【大】 【中】 【小】
甾体药物作为仅次于抗生素的第二大类药物,在抗炎、抗肿瘤、妊娠调节与抗过敏等领域具有重要临床价值。利用葡萄糖等简单生物基碳源从头合成甾体药物,被定义为甾体激素工业3.0(Steroid Hormone Industry 3.0, SHI 3.0),是未来绿色可持续生产的重要方向。该策略的核心依赖于高效酶的发现与优化、高适配性底盘菌及高效微生物细胞工厂的构建。前期研究突破了传统“动物路线”(依赖线粒体复杂转化)的局限,发现了更为高效和简洁的“植物路线”,该路线直接在内质网中利用胆固醇类物质合成甾体激素,并据此创建了“人工本草细胞”,使其能够利用葡萄糖、乙醇等廉价碳源将天然孕激素产量提升至克级每升,效率显著高于“动物路线”。
目前全球上市的甾体药物超过400种,其生物活性高度依赖母核上功能基团的种类与空间位置。在孕激素药物(如地屈孕酮、甲地孕酮、诺美孕酮)和C7-功能化甾体(如氟维司群、米勃龙)的合成中,C6位的脱氢反应至关重要,它既能提升部分孕激素的口服生物利用度,也是C7位引入官能团的“预活化”步骤。然而,能够催化此关键步骤的酶长期未被发现,制约了基于SHI 3.0框架实现非天然孕激素从头合成的发展。
近期,中国科学院天津工业生物技术研究所微生物代谢工程团队从药用植物通关藤(已被开发多种抗肿瘤中药)中鉴定了一个新颖的P450甾体Δ6脱氢酶(MtCYP82BQ1),该酶能催化孕酮在C6位选择性脱氢,生成6-脱氢孕酮,且对多种甾体底物(如17α-羟基黄体酮、睾酮、诺龙等)具有活性。基于此发现,研究人员运用合成生物学技术筛选和搭建了由植物来源的P450甾醇侧链裂解酶CcCYP87N1,3β-羟基类固醇脱氢酶/Δ5-Δ4酮类固醇异构酶CcHSD6,与Δ6-脱氢酶组成的从头生物合成通路,结合基因模块适配、酶工程与代谢工程,构建出能由葡萄糖和乙醇等简单碳源直接发酵生产孕酮与6-脱氢孕酮的“人工本草细胞”,其产量分别达到1.34 g/L与0.72 g/L。这项工作首次实现了非天然孕激素的高效从头合成,为甾体激素工业3.0(SHI 3.0)技术在绿色合成非天然甾体药物方面的巨大潜力提供了实证支持。
该工作获得国家重点研发计划、国家自然科学基金等项目的资助,相关成果发表在Chemical Engineering Journal上,并申请专利2项。天津工生所李荣生博士为该论文的第一作者,天津工生所、国家合成生物技术创新中心戴住波研究员和张学礼研究员为论文的共同通讯作者。
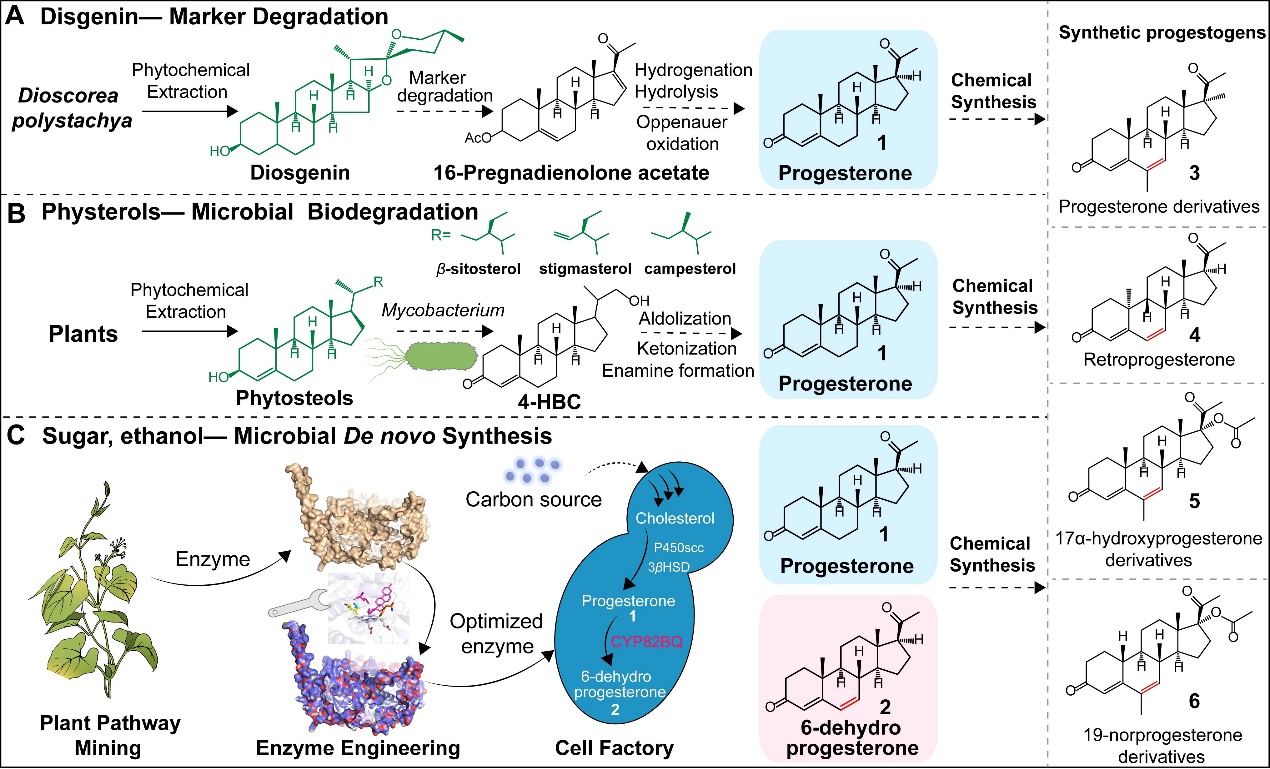
基于甾体激素工业3.0技术框架实现非天然孕激素从头合成
A.薯蓣皂素为原料的Marker降解法(SHI 1.0);B. 植物甾醇为原料的微生物转化的半合成路线(SHI 2.0);C. 基于葡萄糖和乙醇等简单碳源的直接发酵生产路线(SHI 3.0)
版权所有 © 2012- Copyright All Rights Reserved 中国科学院天津工业生物技术研究所 版权所有
通讯地址:天津空港经济区西七道32号,邮编:300308
电话:022-84861997/84861977,传真:022-84861926,邮箱:tib_zh(AT)tib.cas.cn